Representación 3D ADN. Fuente: wikipedia.es
En este blog
- Comentemos... (18)
- Conóceme (1)
- Esquemas y Resúmenes (21)
- Insignias (1)
- Materiales (1)
- Reflexiones y Frases Inspiradoras (8)
Esquema general Tema 6: Los ácidos nucleicos
Practica los ácidos nucleicos
Hola de nuevo!!! :)
En esta entrada os propongo la idea de realizar un juego y así poder aprender y a la vez divertirte jugando:
En esta entrada os propongo la idea de realizar un juego y así poder aprender y a la vez divertirte jugando:
Proteínas
Holaaaa ;)!!!
Aquí os dejo unas preguntas que he realizado sobre las proteínas:
En disolución estas soluciones pueden comportarse como ácido o como base y es muy bueno para la regulación del Ph. El punto isoeléctrico donde el Ph = 7 y la molécula es dipolar.
Aquí os dejo unas preguntas que he realizado sobre las proteínas:
ACTIVIDADES DE PROTEÍNAS
1. Con respecto a las proteínas:
a) Enumerar los cuatro niveles de estructura de las proteínas.
La organización de una proteína viene definida por cuatro niveles estructurales denominados: estructura primaria, que es la estructura más sencilla, es decir, una secuencia lineal de aminoácidos.
Estructura secundaria, es la disposición espacial de la estructura primaria, podemos encontrar: α-hélice (se desarrolla en espiral haciendo giros sobre sí misma, lo que le da la forma de escalera de caracol), conformación-ß (es como una lámina plegada, una cadena se enrolla y varias independientes formando un estructura de zing zang) y la hélice de colágeno (es la unión de 3 hélices y es un ejemplo concreto el colágeno, lo forma 3 aminoácidos y el giro es levógiro, es decir, hacia la izquierda.
Estructura terciaria es la disposición en el espacio de la estructura secundaria, las características y funciones de las proteínas dependen de esta estructura, hay dos tipos: globulares (forma de globo, se enrollan de manera compacta) y fibrosas (cadenas peptídicas y las moléculas son alargadas).
Y estructura cuaternaria es la que presentan las proteínas cuando posee dos o más cadenas polipeptídicas.
Estructura secundaria, es la disposición espacial de la estructura primaria, podemos encontrar: α-hélice (se desarrolla en espiral haciendo giros sobre sí misma, lo que le da la forma de escalera de caracol), conformación-ß (es como una lámina plegada, una cadena se enrolla y varias independientes formando un estructura de zing zang) y la hélice de colágeno (es la unión de 3 hélices y es un ejemplo concreto el colágeno, lo forma 3 aminoácidos y el giro es levógiro, es decir, hacia la izquierda.
Estructura terciaria es la disposición en el espacio de la estructura secundaria, las características y funciones de las proteínas dependen de esta estructura, hay dos tipos: globulares (forma de globo, se enrollan de manera compacta) y fibrosas (cadenas peptídicas y las moléculas son alargadas).
Y estructura cuaternaria es la que presentan las proteínas cuando posee dos o más cadenas polipeptídicas.
b) Indicar qué tipos de enlaces intervienen en la estabilización de cada uno de estos niveles estructurales.
La estructura primaria posee enlaces peptídicos y covalentes.
La estructura secundaria posee enlaces por puentes de hidrógeno, (en la α-hélice se producen enlaces de hidrógeno intracatenarios, es decir dentro de la molécula. En la conformación-ß se producen enlaces de hidrógeno intercatenarios, es decir entre cadenas. En la hélice de hidrógeno la unión se produce por medio de enlaces covalentes y por enlaces débiles de tipo puente de hidrógeno).
En la estructura terciaria pueden ser por: puentes de hidrógeno (enlaces débiles, en los grupos peptídicos), puentes electroestáticos(en grupos de carga opuesta), hidrofóbicos, fuerzas de Van der Waals y enlace covalente de disulfuro (enlace fuerte se produce por ejemplo entre dos cisteínas).
Y por último en la estructura cuaternaria se producen enlaces débiles no covalentes.

Fuente: Google imágenes
La estructura primaria posee enlaces peptídicos y covalentes.
La estructura secundaria posee enlaces por puentes de hidrógeno, (en la α-hélice se producen enlaces de hidrógeno intracatenarios, es decir dentro de la molécula. En la conformación-ß se producen enlaces de hidrógeno intercatenarios, es decir entre cadenas. En la hélice de hidrógeno la unión se produce por medio de enlaces covalentes y por enlaces débiles de tipo puente de hidrógeno).
En la estructura terciaria pueden ser por: puentes de hidrógeno (enlaces débiles, en los grupos peptídicos), puentes electroestáticos(en grupos de carga opuesta), hidrofóbicos, fuerzas de Van der Waals y enlace covalente de disulfuro (enlace fuerte se produce por ejemplo entre dos cisteínas).
Y por último en la estructura cuaternaria se producen enlaces débiles no covalentes.
Fuente: Google imágenes
c) Especificar la estructura que caracteriza a las α-queratinas.
La estructura que caracteriza a este tipo es de estructura secundaria de tipo α-hélice, se desarrolla en espiral posee forma de escalera de caracol es estable porque se producen enlaces de hidrógeno intracatenarios, es decir, dentro de la molécula.
Entre el grupo -NH de un enlace peptídico y el grupo -C=O del 4º aminoácido le da estabilidad. Posee un giro dextrógiro, es decir hacia la derecha, cada aminoácido gira 100º respecto del anterior, en total son 3.6 aminoácidos. Los -C=O se orientan al mismo lado y los -NH hacia el lado contrario. Los radicales dirigidos hacia el exterior de la α-hélice.
La estructura que caracteriza a este tipo es de estructura secundaria de tipo α-hélice, se desarrolla en espiral posee forma de escalera de caracol es estable porque se producen enlaces de hidrógeno intracatenarios, es decir, dentro de la molécula.
Entre el grupo -NH de un enlace peptídico y el grupo -C=O del 4º aminoácido le da estabilidad. Posee un giro dextrógiro, es decir hacia la derecha, cada aminoácido gira 100º respecto del anterior, en total son 3.6 aminoácidos. Los -C=O se orientan al mismo lado y los -NH hacia el lado contrario. Los radicales dirigidos hacia el exterior de la α-hélice.
d) Describir dos propiedades generales de las proteínas.
Solubilidad: Las proteinas son solubles en agua cuando adoptan una conformación globular. La solubilidad es debida a los radicales (-R) libres de los aminoácidos que, al ionizarse, establecen enlaces débiles (puentes de hidrógeno) con las moléculas de agua. Así, cuando una proteina se solubiliza queda recubierta de una capa de moléculas de agua (capa de solvatación) que impide que se pueda unir a otras proteinas lo cual provocaría su precipitación (insolubilización). Esta propiedad es la que hace posible la hidratación de los tejidos de los seres vivos.
Especificidad: Es una de las propiedades más características y se refiere a que cada una de las especies de seres vivos es capaz de fabricar sus propias proteinas (diferentes de las de otras especies) y, aún, dentro de una misma especie hay diferencias protéicas entre los distintos individuos. Esto no ocurre con los glúcidos y lípidos, que son comunes a todos los seres vivos. La enorme diversidad protéica interespecífica e intraespecífica es la consecuencia de las múltiples combinaciones entre los aminoácidos, lo cual está determinado por el ADN de cada individuo. La especificidad de las proteinas explica algunos fenómenos biológicos como: la compatibilidad o no de transplantes de órgános; injertos biológicos; sueros sanguíneos; etc... o los procesos alérgicos e incluso algunas infecciones.
Solubilidad: Las proteinas son solubles en agua cuando adoptan una conformación globular. La solubilidad es debida a los radicales (-R) libres de los aminoácidos que, al ionizarse, establecen enlaces débiles (puentes de hidrógeno) con las moléculas de agua. Así, cuando una proteina se solubiliza queda recubierta de una capa de moléculas de agua (capa de solvatación) que impide que se pueda unir a otras proteinas lo cual provocaría su precipitación (insolubilización). Esta propiedad es la que hace posible la hidratación de los tejidos de los seres vivos.
Especificidad: Es una de las propiedades más características y se refiere a que cada una de las especies de seres vivos es capaz de fabricar sus propias proteinas (diferentes de las de otras especies) y, aún, dentro de una misma especie hay diferencias protéicas entre los distintos individuos. Esto no ocurre con los glúcidos y lípidos, que son comunes a todos los seres vivos. La enorme diversidad protéica interespecífica e intraespecífica es la consecuencia de las múltiples combinaciones entre los aminoácidos, lo cual está determinado por el ADN de cada individuo. La especificidad de las proteinas explica algunos fenómenos biológicos como: la compatibilidad o no de transplantes de órgános; injertos biológicos; sueros sanguíneos; etc... o los procesos alérgicos e incluso algunas infecciones.
e) Describir dos funciones de las proteínas. Indica ejemplo.
Defensa inmunitaria: las inmunoglobulinas dan lugar a los anticuerpos, que se forma como respuesta a la presencia de sustancias extrañas o antígenos, a los que aglutinan o precipitan.

Fuente: Google Imágenes
Movimiento: la contracción muscular se debe a la interacción de filamentos proteicos de actina y miosina.

Fuente: Google Imágenes
Defensa inmunitaria: las inmunoglobulinas dan lugar a los anticuerpos, que se forma como respuesta a la presencia de sustancias extrañas o antígenos, a los que aglutinan o precipitan.
Fuente: Google Imágenes
Movimiento: la contracción muscular se debe a la interacción de filamentos proteicos de actina y miosina.

Fuente: Google Imágenes
f) Defina el proceso de desnaturalización. ¿Qué tipo de enlaces no se ven afectados?
La desnaturalización de una proteína se refiere a la ruptura de los enlaces todos excepto los enlaces peptídicos que mantenían sus estructuras cuaternaria, terciaria y secundaria, conservándose solamente la primaria.
En estos casos las proteínas se transforman en filamentos lineales y delgados que se entrelazan hasta formar compuestos fibrosos e insolubles en agua.
Los agentes que pueden desnaturalizar a una proteína pueden ser: calor excesivo; sustancias que modifican el pH; alteraciones en la concentración; alta salinidad; agitación molecular; etc... El efecto más visible de éste fenómeno es que las proteínas se hacen menos solubles o insolubles y que pierden su actividad biológica.
La mayor parte de las proteínas experimentan desnaturalizaciones cuando se calientan entre 50 y 60 ºC; otras se desnaturalizan también cuando se enfrian por debajo de los 10 a 15 ºC.
La desnaturalización puede ser reversible (renaturalización) pero en muchos casos es irreversible.
g) ¿Qué significa que un aminoácido es anfótero?La desnaturalización de una proteína se refiere a la ruptura de los enlaces todos excepto los enlaces peptídicos que mantenían sus estructuras cuaternaria, terciaria y secundaria, conservándose solamente la primaria.
En estos casos las proteínas se transforman en filamentos lineales y delgados que se entrelazan hasta formar compuestos fibrosos e insolubles en agua.
Los agentes que pueden desnaturalizar a una proteína pueden ser: calor excesivo; sustancias que modifican el pH; alteraciones en la concentración; alta salinidad; agitación molecular; etc... El efecto más visible de éste fenómeno es que las proteínas se hacen menos solubles o insolubles y que pierden su actividad biológica.
La mayor parte de las proteínas experimentan desnaturalizaciones cuando se calientan entre 50 y 60 ºC; otras se desnaturalizan también cuando se enfrian por debajo de los 10 a 15 ºC.
La desnaturalización puede ser reversible (renaturalización) pero en muchos casos es irreversible.
En disolución estas soluciones pueden comportarse como ácido o como base y es muy bueno para la regulación del Ph. El punto isoeléctrico donde el Ph = 7 y la molécula es dipolar.
- Cuando el Ph es elevado y mayor que 7, es un medio básico (actúa como ácido, es decir cede protones). La concentración en el medio (posee baja cantidad de protones y elevada de -OH), es decir hacia la izquierda.
- Cuando el Ph es bajo y menor que 7, es un medio ácido (actúa como base, es decir capta protones). La concentración en el medio (posee elevada cantidad de protones y baja de -OH), es decir hacia la derecha.
Esquema general Tema 5: Las proteínas
Hola una vez más!!!
Hoy os traigo el esquema sobre las proteínas. Espero que os guste!!!
Hoy os traigo el esquema sobre las proteínas. Espero que os guste!!!
Fuente:Propia
En este esquema como podéis observar he partido de la principal idea que son los aminoácidos, ya que son los que forman las proteínas.
En el posit rosa se puede observar la principal estructura de un aminoácido, es decir lo que no varía, excepto la parte de la R, a la que esta estructura se le añade un radical. Después he comentado las propiedades físicas, en el enalce peptídico que es muy importante, el carácter anfótero y los tipos hasta llegar a los polipéptidos que son las proteínas.
Dentro de las proteínas las he dividido en las distintas estructuras: primaria, secundaria, cuaternaria, sobre todo la terciaria que es la estructura de la que dependen las proteínas ya que le atribuyen las características y funciones.
Y por último, como siempre, aquí os dejo un cuestionario, que es realmente útil para estudiar y sobre todo para saber si sabéis de verdad las proteínas:
Fuente: uned.com
Aunque también, podéis realizar las preguntas que nuestra profesora Nieves Moreno nos ha mandado realizar y que podéis hacer vuestra cuenta y después corregirlas en la siguiente entrada.
Adelante!!!!
Fuente: Doña Nieves Moreno, profesora y jefa de estudios de nuestro colegio diocesano Santo Domingo
5 de noviembre- Noche de Guy Fawkes
"Recuerden, recuerden, el 5 de noviembre. Conspiración, pólvora y traición. No veo la demora y siempre es la hora para evocarla sin dilación”.
"Este concierto se lo dedico a la señora Justicia en honor a las vacaciones que parece se está tomando."
"Nos dicen que recordemos los ideales, no al hombre, porque un hombre se puede acabar. Pueden detenerle, pueden matarle, pueden olvidarle, pero 400 años más tarde los ideales pueden seguir cambiando el mundo."
"Mientras pueda utilizarse la fuerza para qué el dialogo. Sin embargo, las palabras siempre conservarán su poder, las palabras hacen posible que algo cobre significado, y si se escuchan, enuncian la verdad."
Fuente: Película "V de Vendetta"
Vídeo
Fuente:Youtube
Guy Fawkes (York, 13 de abril de 1570-Londres, 31 de enero de 1606), fue un conspirador católico inglés. Sirvió en el Ejército Español de los Países Bajos y perteneció a un grupo del Restauracionismo Católico inglés, el cual planeó la Conspiración de la pólvora con el objetivo de volar el Palacio de Westminster con explosivos situados debajo de la Cámara de los Lores y asesinar al rey Jacobo I de Inglaterra, a sus familiares y los lores.
Él era la pieza clave: debía detonar los explosivos cuando los parlamentarios estuviesen reunidos, pero fue arrestado el 5 de noviembre de 1605. Declaró que sus intenciones eran acabar con las persecuciones religiosas, se negó a denunciar a sus cómplices y fue ejecutado. Desde entonces, se rememora ese día como Noche de Guy Fawkes o la Noche de las Hogueras –Bonfire Night en inglés–, donde se simula la quema del mismo en la hoguera.
Fuente: Wikipedia
Hay una película titulada: "V de Vendetta" que está inspirada en este hombre:
Trailer
Fuente:Youtube

Fuente: Google imágenes
Un tiempo después se creó una máscara en su memoria:

Fuente: Google Imágenes
"Este concierto se lo dedico a la señora Justicia en honor a las vacaciones que parece se está tomando."
"Nos dicen que recordemos los ideales, no al hombre, porque un hombre se puede acabar. Pueden detenerle, pueden matarle, pueden olvidarle, pero 400 años más tarde los ideales pueden seguir cambiando el mundo."
"Mientras pueda utilizarse la fuerza para qué el dialogo. Sin embargo, las palabras siempre conservarán su poder, las palabras hacen posible que algo cobre significado, y si se escuchan, enuncian la verdad."
Fuente: Película "V de Vendetta"
Vídeo
Fuente:Youtube
Guy Fawkes (York, 13 de abril de 1570-Londres, 31 de enero de 1606), fue un conspirador católico inglés. Sirvió en el Ejército Español de los Países Bajos y perteneció a un grupo del Restauracionismo Católico inglés, el cual planeó la Conspiración de la pólvora con el objetivo de volar el Palacio de Westminster con explosivos situados debajo de la Cámara de los Lores y asesinar al rey Jacobo I de Inglaterra, a sus familiares y los lores.
Él era la pieza clave: debía detonar los explosivos cuando los parlamentarios estuviesen reunidos, pero fue arrestado el 5 de noviembre de 1605. Declaró que sus intenciones eran acabar con las persecuciones religiosas, se negó a denunciar a sus cómplices y fue ejecutado. Desde entonces, se rememora ese día como Noche de Guy Fawkes o la Noche de las Hogueras –Bonfire Night en inglés–, donde se simula la quema del mismo en la hoguera.
Fuente: Wikipedia
Hay una película titulada: "V de Vendetta" que está inspirada en este hombre:
Trailer
Fuente:Youtube

Fuente: Google imágenes
Un tiempo después se creó una máscara en su memoria:

Fuente: Google Imágenes
Lípidos
Hola de nuevo!!!!
Aquí os dejo las preguntas que he respondido sobre los lípidos, espero que aprendáis mucho:
ACTIVIDADES LÍPIDOS
1. Con respecto a los fosfolípidos:
a) Explique su composición química, haciendo referencia al tipo de enlaces que unen a sus componentes.
Los fosfolípidos son lípidos saponificables, están compuestos por una molécula de glicerina que está unida mediante enlaces éster a dos ácidos grasos a través de los carbonos 1 y 2, y mediante un enlace fosfodiéster a un grupo fosfato por el carbono 3. Además, el grupo fosfato puede formar otro enlace éster con una molécula polar que puede ser un aminoalcohol o un polialcohol.
b) ¿En qué estructura celular se localizan mayoritariamente los fosfolípidos?
Los fosfolípidos son los principales componentes de las membranas celulares.
c) Explique qué significa que los fosfolípidos son compuestos anfipáticos y su implicación en la organización de dicha estructura.
Los fosfolípidos son moléculas anfipáticas, es decir, poseen una zona polar hidrofílica y otra zona apolar hidrofóbica. La naturaleza anfipática de los fosfolípidos les proporciona un papel fundamental en la formación de las membranas celulares, tanto de las células procariotas como de las eucariotas. La membrana celular está constituida por una bicapa lípidica donde en las cadenas hidrofóbicas de los fosfolípidos se orientan hacia el interior, mientras que las cabezas polares están en contacto con el medio acuoso existente a ambos lados de la membrana.
2. Los lípidos son moléculas orgánicas presentes en todos los seres vivos con una gran heterogeneidad de funciones.
a) Indique la composición química de un triacilglicérido de origen vegetal.
Los triacilglicéridos son lípidos saponificables formados por la esterificación de la glicerina con tres
ácidos grasos. A temperatura ambiente, pueden ser sólidos (forman los denominados sebos) y
líquidos (forman aceites en los vegetales). Se tratan de lípidos simples, ya que no presentan más
componentes.
b) La obtención del jabón se basa en una reacción en la que intervienen algunos lípidos; explique esta reacción e indique cómo se denomina.
El proceso es el de saponificación, que se produce por la reacción del triacilglicérido con una base (álcali), formándose la sal correspondiente, el jabón y la glicerina.
c) Justifique si el aceite de oliva empleado en la cocina podría utilizarse para la obtención de jabón.
Sí se podría ya que, el aceite de oliva empleado en la cocina es un lípido saponificable por lo tanto todos los lípidos saponificables se pueden utilizar para la obtención de jabón.
3. Dada la siguiente estructura indique:
a)¿Qué tipo de molécula se muestra?
La molécula que se nos presenta es un triacilglicérido.
Los triacilglicéridos o también se les conoce como grasas neutras por lo tanto son apolares, saponificables, insolubles en compuestos polares y su principal función es de reserva energética.
c) En los organismos vivos animales y vegetales ¿dónde encontraría este tipo de moléculas?
Este tipo de lípidos son la fuente principal de reserva energética en animales que se suelen almacenar en el tejido adiposo y en los vegetales se almacenan en las vacuolas.
Las "grasas" se almacenan para su uso pero para largo período, ya que no son las únicas biomoléculas orgánicas que aportan energía, el organismo para obtener energía utiliza primeramente los glúcidos (que son las biomoléculas del tema anterior) y después cuando no dispone de glúcidos, utiliza los lípidos.
Espero que os haya gustado. Hasta la próxima!!!
Espero que os haya gustado. Hasta la próxima!!!
Esquema General Tema 4: Los Lípidos
Hola chic@s!!!!
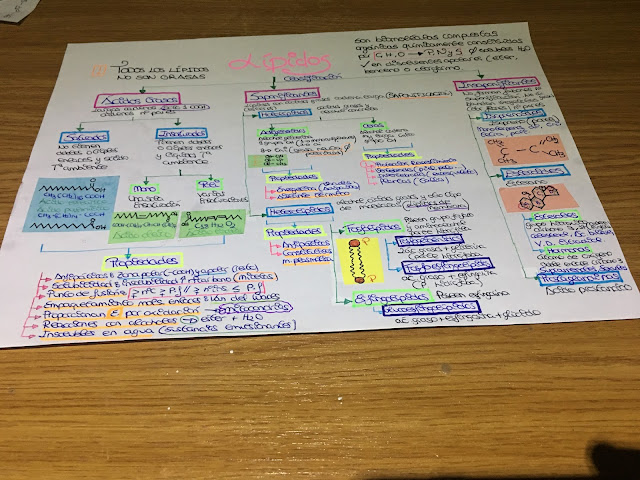
Hoy os traigo el esquema general que he realizado sobre los lípidos:
Como podéis observar he partido de la idea de los lípidos y he sacado 3 flechas con los tres tipos que son ácidos grasos, saponificables e insaponificables. Los posits de colores son ejemplos que he puesto sobre los distintos tipos ya que así me ayudan a estudiar.
Si queréis comprobar si habéis entendido a la perfección aquí os dejo un test de preguntas que he encontrado realmente interesante:
Cuestionario
Fuente: www.uned.es
Y también podéis realizar estas preguntas por vuestra cuenta y en la siguiente entrada podéis corregirlas:
Actividades
Fuente: Doña Nieves Moreno, jefa de estudios y profesora de biología de nuestro colegio diocesano Santo Domingo.
Adelante!!! Así podréis saber si realmente habéis entendido los lípidos o necesitáis darles un último repasillo
Hoy os traigo el esquema general que he realizado sobre los lípidos:
Como podéis observar he partido de la idea de los lípidos y he sacado 3 flechas con los tres tipos que son ácidos grasos, saponificables e insaponificables. Los posits de colores son ejemplos que he puesto sobre los distintos tipos ya que así me ayudan a estudiar.
Si queréis comprobar si habéis entendido a la perfección aquí os dejo un test de preguntas que he encontrado realmente interesante:
Cuestionario
Fuente: www.uned.es
Y también podéis realizar estas preguntas por vuestra cuenta y en la siguiente entrada podéis corregirlas:
Actividades
Fuente: Doña Nieves Moreno, jefa de estudios y profesora de biología de nuestro colegio diocesano Santo Domingo.
Adelante!!! Así podréis saber si realmente habéis entendido los lípidos o necesitáis darles un último repasillo
Vídeo para reflexionar
Hola chic@s!!!!
He encontrado un vídeo realmente interesante y te invita a la reflexión. Espero que os guste:
Vídeo
Fuente: Youtube
He encontrado un vídeo realmente interesante y te invita a la reflexión. Espero que os guste:
Vídeo
Fuente: Youtube
Experiencia en el LABORATORIO!!!!
Hola a tod@s!!!
El pasado martes acudimos al laboratorio para hacer la práctica del reactivo de Fehling. Me ha parecido una experiencia increíble!!!
Nuestro experimento lo hemos realizado con:
A continuación os dejo el informe de la práctica:
Informe
Y a continuación voy a contestar las preguntas propuestas en el informe de la práctica:
Una cosa que se puede realizar es con la muestra de orina introducir un poco de reactivo de Fehling y si se produce reacción es que sí hay glucosa, por lo tanto esa persona podría ser diabética.
A continuación unas imágenes en el laboratorio:
El pasado martes acudimos al laboratorio para hacer la práctica del reactivo de Fehling. Me ha parecido una experiencia increíble!!!
Nuestro experimento lo hemos realizado con:
- Glucosa
- Sacarosa
- Cerveza
- Zumo
A continuación os dejo el informe de la práctica:
Informe
Y a continuación voy a contestar las preguntas propuestas en el informe de la práctica:
1. ¿Qué azúcares son reductores? ¿Por qué?
Los azúcares reductores son aquellos azúcares que poseen el grupo -OH hemiacetálico libre, por lo que dan positivo a la reacción con reactivo de Fehling. En nuestra práctica los azúcares reductores han sido:
La glucosa, el zumo y la cerveza que nos indica una coloración rojo ladrillo a diferente nivel de coloración ya que esto se debe a la concentración de azúcar en cada solución, estableciendo que se produjo la reducción y que la prueba fue positivo.
2. ¿Qué ocurre en el tubo 2? y ¿en el 10?
En el tubo 2 la solución de azúcar reductor es la sacarosa el resultado nos indica una coloración azul determinando que esta solución es un azúcar no reductor debido a que la prueba salio negativa y que no se produjo la reducción.
Esto se da porque es un azúcar constituida por una molécula de glucosa y de fructosa, tiene un enlace entre el primer carbono de la glucosa y el segundo carbono de la fructosa, y no queda grupos reductores disponibles. Al no ser reductor, la prueba de Fehling es negativa, y por lo que se intuye, no posee el grupo carbonilo apto y libre, necesario como para reaccionar con el reactivo Fehling.
En el tubo 2 la solución de azúcar reductor es la sacarosa el resultado nos indica una coloración azul determinando que esta solución es un azúcar no reductor debido a que la prueba salio negativa y que no se produjo la reducción.
Esto se da porque es un azúcar constituida por una molécula de glucosa y de fructosa, tiene un enlace entre el primer carbono de la glucosa y el segundo carbono de la fructosa, y no queda grupos reductores disponibles. Al no ser reductor, la prueba de Fehling es negativa, y por lo que se intuye, no posee el grupo carbonilo apto y libre, necesario como para reaccionar con el reactivo Fehling.
Por otra parte, al añadir ácido clorhídrico a la sacarosa, calentarlo al baño maría y añadir a la mezcla "sosa" para neutralizar el ácido, se produce la hidrólisis de la sacarosa. Cuando volvemos a calentar el tubo se produce la reacción, ya que la sacarosa se ha hidrolizado en glucosa y fructosa, que estos sí son reductores.
3. ¿Qué función tiene el ácido clorhídrico?
El ácido clorhídrico es realmente importante ya que permite hidrolizar la sacarosa en glucosa y fructosa.
El ácido clorhídrico es realmente importante ya que permite hidrolizar la sacarosa en glucosa y fructosa.
4. ¿Dónde produce nuestro cuerpo ácido clorhídrico?
El HCl es uno de los muchos químicos liberados en nuestro estómago cuando consumimos alimentos. El papel del ácido clorhídrico en el estómago, junto con los otros jugos gástricos, es descomponer los alimentos y causar la liberación de enzimas que después ayudan a la digestión.
5. Los diabéticos eliminan glucosa por la orina ¿Cómo se puede diagnosticar la enfermedad?
El HCl es uno de los muchos químicos liberados en nuestro estómago cuando consumimos alimentos. El papel del ácido clorhídrico en el estómago, junto con los otros jugos gástricos, es descomponer los alimentos y causar la liberación de enzimas que después ayudan a la digestión.
5. Los diabéticos eliminan glucosa por la orina ¿Cómo se puede diagnosticar la enfermedad?
Una cosa que se puede realizar es con la muestra de orina introducir un poco de reactivo de Fehling y si se produce reacción es que sí hay glucosa, por lo tanto esa persona podría ser diabética.
A continuación unas imágenes en el laboratorio:
Calentando el agua para el baño maría
Añadiendo el reactivo
Calentándolo al baño maría, utilizando pinzas
Se puede observar el color ladrillo después de calentar al baño maría la cerveza y el zumo
Conclusiones:
- La prueba de Fehling nos permite identificar cual es un azúcar reductor.
- La mayoría de los monosacáridos y algunos disacáridos poseen poder reductor.
- Un azúcar es reductor por la formación de un precipitado de color rojo ladrillo (óxido cuproso) y la decoloración de la solución.
- Podemos concluir que las muestras de glucosa, fructosa, maltosa y galactosa son azúcares reductores, ya que se formó un precipitado de color rojo ladrillo (óxido cuproso).
- En cambio la sacarosa es un azúcar no reductor, debido a que no se formó un precipitado de color rojo ladrillo.
Glúcidos
A continuación os dejo unas preguntas sobre los glúcidos con sus correspondientes respuestas en color rosa.
ACTIVIDADES GLÚCIDOS
1) La D-glucosa es una aldohexosa.
Explica:
a) ¿Qué significa ese término?
La glucosa es un glúcido es decir que posee un grupo carbonilo que puede ser aldheído (si se encuentra en el extremo de cadena) o cetona ( si se encuentra en interior de cadena). Más concretamente la glucosa es un monosacárido es decir que están constituidos por una única cadena, donde la molécula puede tener de 3 a 7 átomos de Carbono y se nombran con la palabra -OSA al final. Por lo tanto, analizando la palabra aldohexosa, por "aldo" llegamos a la conclusión de que es un aldehído, por "hex" quiere decir que posee 6 átomos de carbono y como he comentado le añadimos la palabra OSA.
b) ¿Qué importancia biológica tiene la glucosa?
La glucosa es la principal fuente de energía del cuerpo, sin ella ninguna función biológica se podría llevar a cabo en nuestros órganos, además es una especie de combustible que te permite realizar tus actividades diarias.
c) ¿Qué diferencia existe entre la D-glucosa y la L-glucosa, y entre la α y la β D- glucopiranosa?
Los monosacáridos poseen propiedades físicas entre ellas se encuentra el carbono asimétrico o quiral que es aquel átomo de carbono que está unido a cuatro grupos diferentes. Entonces, para diferenciar entre D y L nos tenemos que fijar en el último y más alejado carbono asimétrico del grupo carbonilo (-CHO) y si en ese carbono el -OH se encuentra a la derecha se escribe D y si el -OH está a la izquierda L.
Como comenté en el vídeo de la explicación del esquema de los glúcidos, cuando ciclamos una molécula se une el OH del carbono asimétrico con el grupo carbonilo entonces, lo que sucede es que se une el carbono 5 con el 1 y el carbono 6 se queda como un radical del carbono 5, por otro lado el carbono 1 tiene dos radicales, un hidrógeno y un OH. Entonces si el radical del carbono 5 que es el carbono 6 se encuentra hacia arriba y el OH del carbono 1 también es decir, en el mismo plano se conoce como β o cis y si se encuentran en diferente plano se le conoce como α o trans.
2) Dentro de un grupo de biomoléculas orgánicas se puede establecer la clasificación de:
monosacáridos, oligosacáridos y polisacáridos.
Homopolisacáridos y heteropolisacáridos
Función energética (reserva) y función estructural.
a) cita un ejemplo diferente para cada uno de los tipos diferenciados en la clasificación 1, 2 y 3 (total 7 moléculas).
Un ejemplo de monosacárido es la L-Glucosa. Un ejemplo de oligosacárido es la maltosa y un ejemplo de polisacárido es la quitina.
Un ejemplo de homopolisacárido es el almidón y un ejemplo de heteropolisacárido es el agar.
Un ejemplo de función energética en lo que se refiere a la reserva es el glucógeno y un ejemplo de función estructural es la celulosa.
b) ¿En base a qué criterio se establece la clasificación número 2 ?
Dentro del grupo holósidos y más concretamente los polisacáridos que son cadenas de más de diez piezas de monosacáridos. Hay dos grupos los homopolisacáridos que están formados por los mismos monosacáridos mientras que los heteropolisacáridos está formados por distintos monosacáridos.
3) En relación a los glúcidos:
a) Indica cuál de los siguientes compuestos son monosacáridos, disacáridos o polisacáridos: sacarosa, fructosa, almidón, lactosa, celulosa y glucógeno.
La sacarosa es un disacárido es decir la unión de un monosacárido y otro monosacárido.
La fructosa es un monosacárido
El almidón es un polisacárido
La lactosa es un disacárido
La celulosa es un polisacárido
El glucógeno es un polisacárido también
b) Indica en qué tipo de organismos se encuentran los polisacáridos indicados en el apartado anterior.
El almidón y la celulosa se encuentran en los vegetales, mientras que el glucógeno se encuentra en animales.
c) Indica cuál es la función principal de los polisacáridos indicados en el apartado a).
El almidón es un polisacárido de reserva energética en las plantas. La celulosa posee la función de sostén en los vegetales también. Pero, el glucógeno es la forma de reserva energética de los animales y se almacena en el hígado y en los músculos.
d) Cita un monosacárido que conozcas y que no se encuentre en la relación incluida en el apartado a).
Por ejemplo la galactosa que se produce por la hidrólisis de la lactosa y de otros polisacáridos
4) Realiza todos los pasos de la ciclación de una D-galactosa hasta llegar a una α-D- galactopiranosa.
Aquí os dejo un vídeo donde explico el proceso de ciclación que he realizado:
Suscribirse a:
Entradas (Atom)